Şaperon Proteinleri İşini Ciddiye Alır
Şaperon proteinleri, ısı şok proteini veya HSP proteini olarak da adlandırılırlar. Şaperon proteinleri genelde ribozomda protein sentezinin son aşamasında yani proteinlerin katlanmasından sorumludur.
Şaperon proteinleri tarafından katlanmayan proteinlerin büyük bir kısmı işlevsizdir.
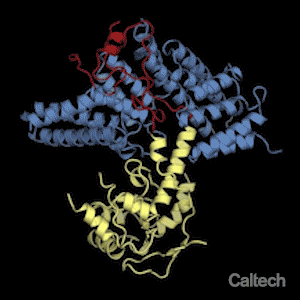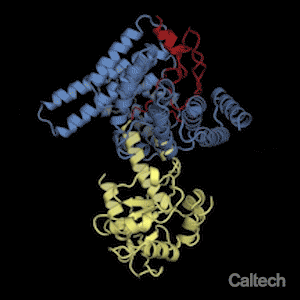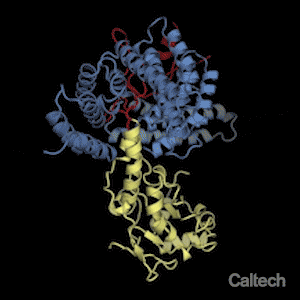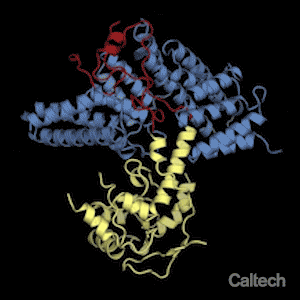
Şaperonuna (mavi) bağlı bir ribozomal proteinin (sarı ve kırmızı) yapısal gösterimi. André Hoelz'in laboratuarında lisansüstü öğrencisi olan Ferdinand Huber, birbirleriyle etkileşime giren protein çiftinin atomik çözünürlükte bir şipşak fotoğrafını yakalayarak, şaperonların sıkıca paketleyerek ribozomal proteinlerini koruyabileceğini ortaya koydu. Ribozom montajı sırasında; şaperondan, ribozomal protein serbest bırakıldığı zaman, şekildeki kırmızı bölgede etkileyici bir şekil değişikliği meydana gelir. Credit: Huber and Hoelz/Caltech
Proteinler için, bu, kırmızı halı muamelesine eşdeğer olur: her bir protein ribozomun (protein üreten hücre organeli) karmaşık mekanizmasına aittir, kendi şaperonu doğru yerde ve doğru zamanda onun zarar görmesini engeller.
Yeni bir Caltech çalışmasında, araştırmacılar, ribozom şaperonlarının nasıl çalıştığı hakkında daha fazla bilgi sahibi oludular. Çalışmaların gösterdiği üzere; özel bir şaperon, sıkı bir şekilde, neredeyse eli tutan bir eldiven gibi çok özel bir şekilde onun proteinine bağlanıyor. Araştırmacılar, şaperonuna bağlı olan ribozomal proteinin atomik yapısını çözmek için X-ışını kristalografisini kullandılar.
Caltech'te kimya profesörü Miras Tıbbi Araştırma Enstitüsü (HMRI) Araştırmacı ve Howard Hughes Tıp Enstitüsü (HHMI) Öğretim Üyesi olan André Hoelz: “Ribozomların yaptığı bir bakıma kek pişirmeye benzer. Bireysel bileşenler, özellikle onların ölçüsüne ve şekline uygun olarak koruyucu ambalajlarda gelirler sonunda bir sulu hamur içinde açılıp karıştırılıncaya kadar.” diyor. “Yaptığımız, koruyucu ambalajın bir ribozomal proteine nasıl uyduğunu ve ambalajın nasıl açıldığını anlamamızdır.” Hoelz, Nature Communications dergisinde 2 Şubat 2017'de yayınlanan araştırmanın arkasındaki baş araştırmacıdır. Bulgu, özellikle ribozom montajını devre dışı bırakmak üzere tasarlanmış yeni kanser ilaçlarının geliştirilmesinde potansiyel uygulamalar içeriyor.
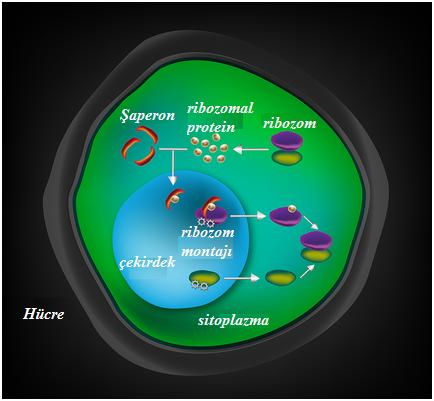
Şaperon proteinlerinin (kırmızı) çekirdeğe ribozomal proteinleri (bej) nakletme sürecini gösteren hücre diyagramı. Şaperonlar ribozomal proteinlere bağlanır ve onları çekirdeğe yönlendirirken proteinleri ayıklama mekanizmasından da korur. Bir ribozomal protein gelişen bir ribozoma (yeşil ve mor) ulaştığında, şaperon bu proteinleri bırakır. Neredeyse komple tamamlanmış ribozom üniteleri final montajına geçmek için çekirdekten çıkarlar. Credit: Huber and Hoelz/Caltech
Tüm hücrelerde genetik bilgiler DNA olarak depolanır ve proteinleri kodlayan mRNA'lara aktarılır. Ribozomlarda tercüme edilen mRNA’lar daki bilgiler ile aminoasitler birbirine bağlanarak polipeptitlere ve onlarda katlanarak proteinlere dönüştürülür. Bir hayvan hücresinde günde bir milyondan fazla ribozom üretilir.
Hücre için ribozom inşası; ribozomun kendisini oluşturan yaklaşık 80 protein, ribozomal RNA dizileri ve süreci yönlendiren ve düzenleyen 200'den fazla ilave proteinden oluşan müthiş bir girişimdir.
Hoelz: Ribozom montajı her şey belirli bir sırada olduğu dinamik bir süreçtir. Şu an sadece ilgili adımları aydınlatmaya başlıyoruz.
Konuyu daha karmaşık hale getirmek için, bir ribozomu oluşturan proteinler önce hücrenin çekirdeğinin dışında, sitoplâzmada sentezlenir, çekirdeğe taşınmadan önce ribozomun başlangıç aşamalarının montajı yapılır.
Şaperon proteinleri, ribozomal proteinlerin hücrenin protein parçalama mekanizması ile parçalanmasını önleyerek çekirdeğe taşınmasına yardımcı olur. Caltech'te biyoloji profesörü Raymond Deshaies ve bir HHMI Araştırmacı tarafından yakın zamanda tanımlanan, bu mekanizmada korumasız ribozomal proteinlerde özel olarak hedefleyen bileşenler, bir ribozomun muazzam yapısını oluşturmak için eşit sayıda ribozomal proteinin mevcut olmasını sağlar.
Bundan önce Hoelz ve ekibi; Heidelberg Üniversitesi'nden Ed Hurt laboratuvarı ile işbirliği yaparak, L4 olarak adlandırılan bir ribozomal proteininin "RpL4'ün Montaj şaperonu" veya Acl4 adlı bir şaperona bağlandığını keşfetti. Şaperon, L4 proteinini çekirdeğe götürürken zarar görmesini engeller ve kesin zaman ve yerde gelişmekte olan ribozama teslim eder. Yeni çalışmada ekip, protein kristallerinin yüksek enerjili X-ışınlarına maruz bırakılmasını içeren bir süreç olan X-ışını kristalografisini kullanarak bağlı çiftin yapısını çözdü. Teknik Stanford Synchrotron Radiation Lightsource’de Caltech'in Moleküler Gözlemevi’nde ışın çizgisi ile gerçekleştirildi.
Hoelz laboratuvarındaki Caltech de lisansüstü öğrencisi Ferdinand Huber ve yeni çalışmanın başyazarı "Bu çözülmesi kolay bir yapı değildi" diyor. “Yapıyı çözmek inanılmaz derecede heyecan vericiydi, çünkü şaperonun korumak için ribozomal proteini nasıl kucakladığını ilk bakışta gözlerimizle görebiliyorduk.” Diye ekliyor.
Hoelz yapının sürpriz olduğunu söylüyor çünkü daha önce şaperonların ribozomal proteinlerini çok sıkı tuttuğu bilinmiyordu. Ribozomal proteinleri sıkıca korumak için benzer şekilde işlev görüp görmediklerini görmek için gelecekte başka şaperonlarla çalışmak istediklerini söyledi.
Sonuçlar, kanser hücrelerinin tümör büyümesi için gerekli sayıda ribozomu tedarik etmesini önleyerek kanser tedavisi için yeni ilaçların geliştirilmesine önderlik edebilir.
"Ribozomal Protein L4'ün Hücresel Degradasyondan Korunması için Moleküler Temeller" adı verilen çalışma, Boehringer Ingelheim Fonds'un doktora bursuyla, Howard Hughes Tıbbi Araştırma Enstitüsünün Fakülte Akademisyen Ödülü, bir Miras Tıbbi Araştırma Enstitüsü Baş Araştırmacı, Sidney Kimmel Kanser Araştırmaları Vakfı'ndan Kimmel Akademik Ödülü, Camille & Henry Dreyfus Vakfı'nın Teacher-Scholar Ödülü ve Caltech'in başlangıç fonları ile finanse edildi.
Çeviri: Barış Uçar Bilime Yön Veren Cevaplar
Kaynaklar: https://phys.org/news/2017-02-protein-chaperone-job.html#nRlv 09.02.2017
More information: Ferdinand M. Huber et al. Molecular basis for protection of ribosomal protein L4 from cellular degradation, Nature Communications (2017). DOI: 10.1038/ncomms14354
Journal reference: Nature Communications
Genetik Haberleri
-
Bugün 16 Nisan Dünya Biyologlar Günü!
-
Allopatrik türleşme nedir ? Nasıl Gelişir ?
-
Maryland’teki “Kölelerin” Yaşayan 42.000 Akrabası Bulundu
-
Araştırmacılar kediler, yunuslar, kuşlar ve düzinelerce başka hayvanın genom haritasını çıkarıyor
-
Kolombiya'da nadir görülen bir kuş türünde "gynandromorphy" gözlemlendi
-
Kurumaya dayanıklı bitkiler için genom veritabanı yayınlandı
-
En son DNA barkodlama teknolojisiyle İsrail'in tatlı su balık türleri listesinin yeniden gözden geçirilmesi
-
İnsanların Daha Önce Bilinmeyen Bir Dokunma Duyusu Keşfedildi
-
Bilim İnsanları Tüm İnsan Genomunun Dizilimini Çıkardı. Ancak Henüz Bitmedi
-
İlk Defa Tazmanya Kaplanından RNA Elde Edildi
-
Neandertal DNA’nız, Sizi Acıya Karşı Daha Hassas Yapıyor Olabilir
-
Epigenetik ve Epigenetik Mekanizmalar
-
İlk taslaktan 20 yıl sonra insan Y kromozomu tamamen dizilendi.
-
Kim Bu Kimerizm? Tek Bedende İki Kişi
-
Gen terapi, genetik materyalin yeniden düzenlenmesi